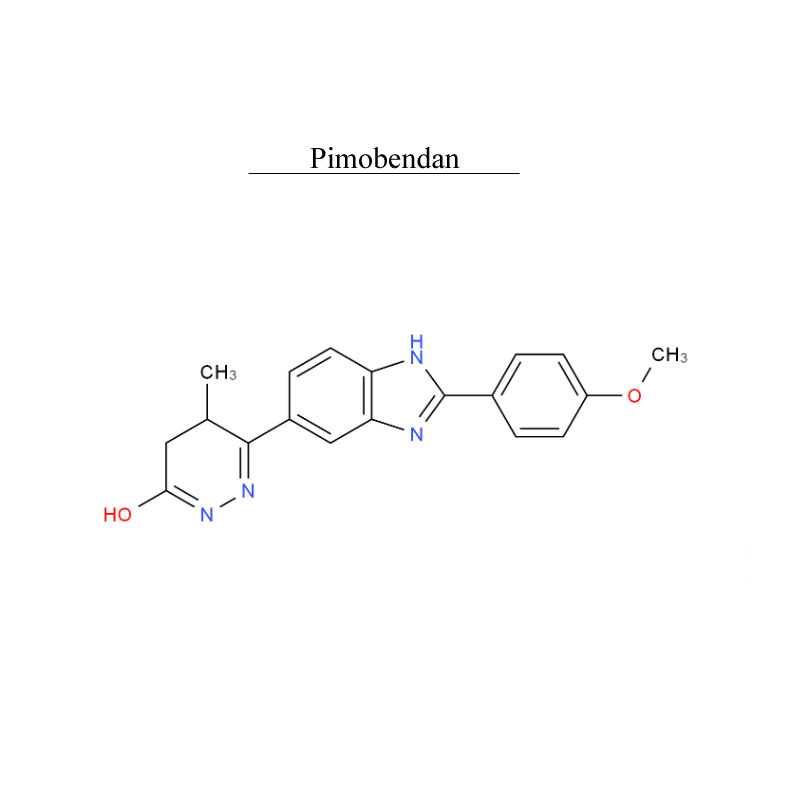
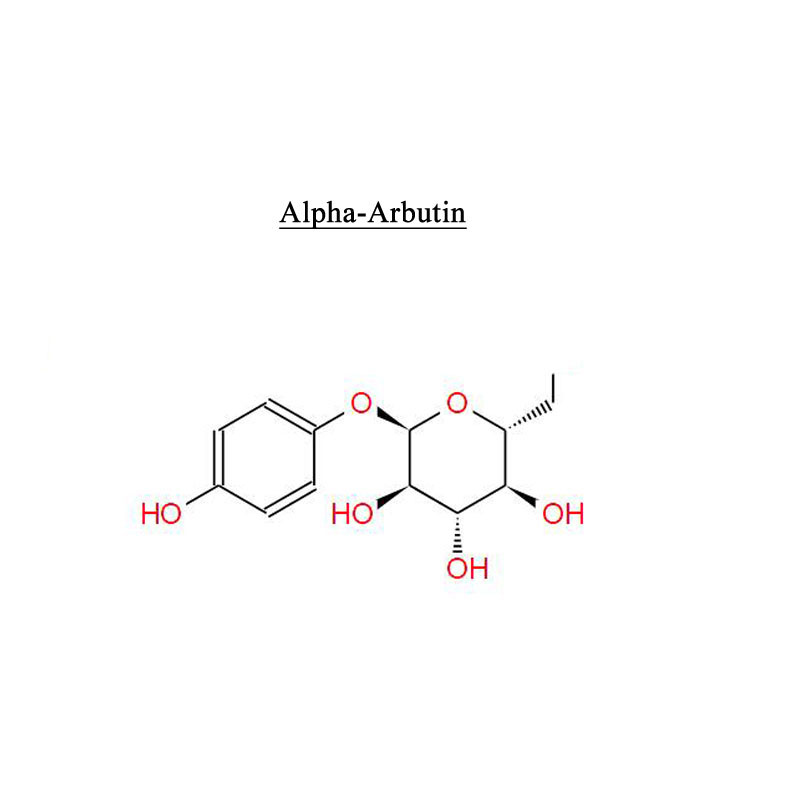
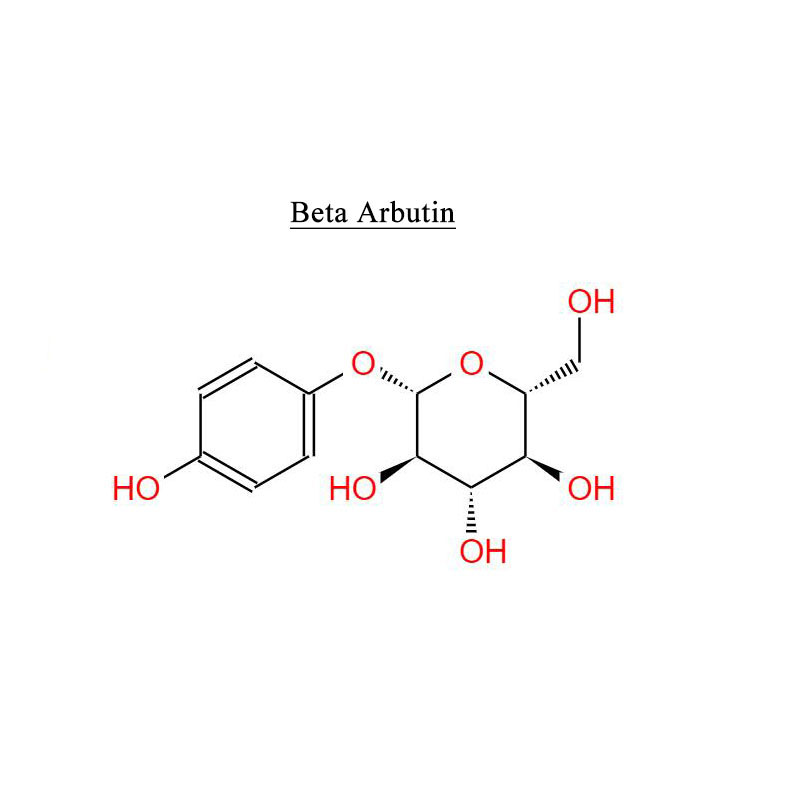
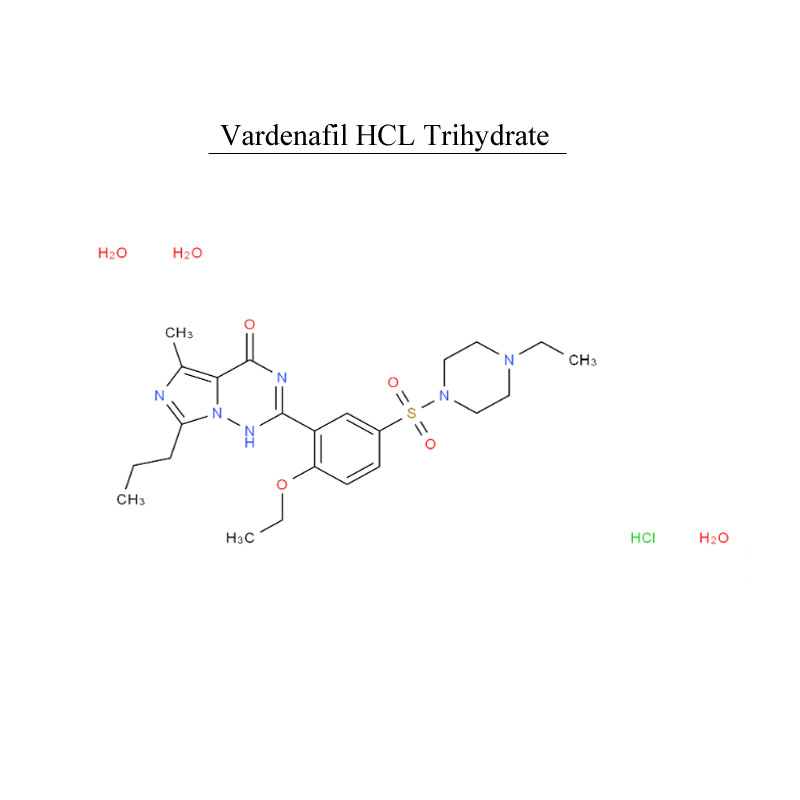
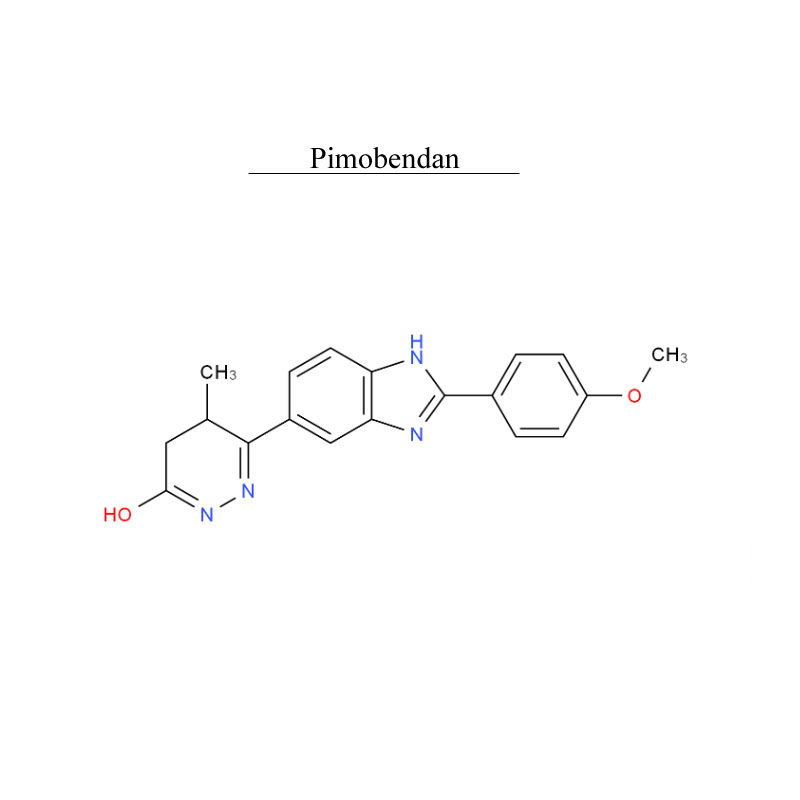
Pimobendan 74150-27-9 Chất ức chế chuyển hóa PDE
Sự chi trả:T/T, L/C
Xuất xứ sản phẩm:Trung Quốc
Cảng giao dịch:Bắc Kinh/Thượng Hải/Hàng Châu
Đơn hàng (MOQ):1g
Thời gian dẫn:3 ngày làm việc
Khả năng sản xuất:1kg/tháng
Điều kiện bảo quản:Bảo quản nơi khô ráo, thoáng mát, nhiệt độ phòng.
Vật liệu đóng gói:lọ, chai
Kích cỡ gói:1g/lọ, 5/lọ, 10g/lọ, 50g/chai, 500g/chai
Thông tin an toàn:LHQ 2811 6.1/PG 3
Giới thiệu
Pimobendan, là một loại thuốc thú y.Nó là một chất nhạy cảm với canxi và là chất ức chế chọn lọc phosphodiesterase 3 (PDE3) với tác dụng tăng co bóp và giãn mạch tích cực.
Pimobendan được sử dụng trong điều trị suy tim ở chó, nguyên nhân phổ biến nhất là do bệnh van hai lá myxomatous (trước đây gọi là bệnh nội tâm mạc) hoặc bệnh cơ tim giãn nở.Nghiên cứu đã chỉ ra rằng dưới dạng đơn trị liệu, pimobendan làm tăng thời gian sống sót và cải thiện chất lượng cuộc sống ở bệnh nhân chó bị suy tim sung huyết thứ phát do bệnh van hai lá khi so sánh với benazepril, một chất ức chế ACE.
Đặc điểm kỹ thuật (USP43)
| Mục | Sự chỉ rõ |
| Vẻ bề ngoài | Bột màu trắng hoặc hơi vàng, hút ẩm |
| Mp | Khoảng 242oC |
| độ hòa tan | Thực tế không hòa tan trong nước, hòa tan tự do trong dimethylformamide, ít tan trong axeton và trong methanil. |
| Nhận biết | Đo quang phổ hấp thụ hồng ngoại, So sánh pimobendan CRS. |
| Thời gian lưu của pic chính của dung dịch mẫu tương ứng với thời gian lưu của dung dịch chuẩn gốc, thu được trong phép thử Tạp chất hữu cơ. | |
| Kim loại nặng | 10ppm |
| Độ chi tiết | P90 25μm |
| Kích thước hạt | Lưới 20-80 |
| Dung môi dư | 500 trang/phút |
| Nước | 1,0% |
| xét nghiệm | 98,0%~102,0% |
| Tro sunfat | 0,10% |
| Các chất liên quan (HPLC) | |
| tạp chất A | 0,10% |
| tạp chất B | 0,10% |
| Bất kỳ tạp chất nào khác | 0,10% |
| Tổng tạp chất | 0,20% |